Wiedza w pigułce
Kwas poli-D,L-mlekowy (PDLLA) to syntetyczny, biokompatybilny, biodegradowalny polimer.
W przypadku augmentacji tkanek miękkich, rozmiar i właściwości chemiczne mikrocząsteczki PDLLA są kluczowe dla zdolności tego środka do promowania subklinicznej odpowiedzi zapalnej, która stymuluje odkładanie kolagenu w zewnątrzkomórkowej matrycy.
Wynikające z tego przywrócenie objętości twarzy następuje w kontrolowany, przewidywalny sposób i jest długotrwałe.
Unikalne fizykochemiczne właściwości biostymulujące PDLLA odróżniają go od innych dostępnych metod leczenia i są podstawą wymaganej unikalnej metodyki leczenia dla optymalnych rezultatów.
Iniekcja kawasu polimlekowego wywołuje w tkance podskórnej reakcję biologiczną, podobną, ale o mniejszym odczynie zapalnym do tej, którą widujemy podczas gojenia ran i zakładania szwów chirurgicznych. Następuje tu naturalne przejście od zapalenia ostrego do zapalenia przewlekłego małego stopnia.
- Zamierzona reakcja zapalna wokół ciała obcego,
- Fibroplazja (rozrost tkanki łącznej włóknistej) w skórze,
- Kolagenogeneza pobudzona przez uwolnione do tkanek mleczany oraz powolna degradacja mikrocząsteczek PDLLA to te czynniki, które w różnym stopniu składają się na długotrwały efekt kliniczny utrzymujący się po zabiegu.
Odpowiedź zapalna na ciało obce, prowadzi do otorbienia mikrocząstek, a następnie fibroplazja i wynikłe odkładanie kolagenu typu I w przestrzeni zewnątrzkomórkowej.
Etapy:
- Odpowiedź tkanek na PDLLA od ostrego stanu zapalnego do słabnącej odpowied zapalna.
- Adsorpcja białek występuje bezpośrednio po wstrzyknięciu, po którym następuje infiltracja przez neutrofile, a następnie makrofagi.
- Degradacja PDLLA, i akumulacja kolagenu w czasie.
- Po 6 miesiącach liczba makrofagów i fibrocytów maleje (Fibrocyt – komórka tkanki łącznej występująca jako zredukowana forma fibroblastu o mniejszej sprawności metabolicznej – komórka starcza , zużyta)
- Produkcja kolagenu nadal rośnie , a stan zapalny wraca do poziomu wyjściowego
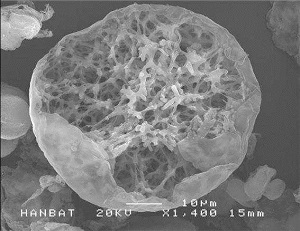
Cząsteczki LENISNA & JUVELOOK są wystarczająco duże, aby uniknąć fagocytozy poprzez makrofagi w skórze, lub też przeniknąć przez ścianki naczyń włosowatych, lecz jednocześnie są wystarczająco małe, aby mogły zostać z łatwością wstrzyknięte za pomocą igły bez jej zatykania. Nie powodują powstawania grudek pod skórą z uwagi na swój okrągły i porowaty kształt.

Zabieg należy powtórzyć 2/3 razy w odstępach od 6 do 8 tygodni. Trwałość zabiegu od ostatniej wizyty przekracza 24 miesiące.
Można znaleźć w literaturze opisy korzystnego działania kawasu polimlekowego u pacjentów nawet przez 40 miesięcy. Odsetek zadowolonych pacjentów przewyższa 90%.
Cząsteczki kwasu poli L mlekowego mają strukturę potłuczonego szkła, a mikrocząstki kwasu poli D,L mlekowego są okrągłe, porowate o strukturze siateczkowatej. Ta wyjątkowa budowa cząsteczek umożliwia połączenie się z nieusieciowanym kwasem hialuronowym co czyni ten preparat wyjątkowym.


- Patent : No. 10-1481441 Manufacturing method of polymeric microparticles having network structure – Metoda wytwarzania mikrocząstek polimerowych o strukturze sieciowej
- Patent : No. 10-1725279 A process for the preparation of polylactic acid microparticles by a spray method –
Proces otrzymywania mikrocząstek kwasu polimlekowego metodą natryskową – kształt kulisty , porowaty
- A comparison between hyaluronic acid and polylactic acid filler injections for temporary penile augmentation in patients with small penis syndrome. Authors: Dae Yul Yang, MD Phd; Hyun Cheol Jeong , MD,; Sun Tae Ahn, MD, PhD; Woong Jin Bae, MD, Phd; Du Geon Moon, MD, PhD; Sae Woong Kim, MD, PhD, and Won Ki Lee, MD, PhD
- Biostymulatory effects of polydioxanonoe, PDLLA and polycaprolactone fillers in mouse model. Authors Tae-Rin Kwon PhD, Sung Won Han MS; In Kwon Yeo MD, Jong Hwan Kim MS, Jae Min Kim MD, Ji-Yeon Hong MD, Byung-Chul Lee MS, Sung-Eun Lee MS, Ho Sang Moon PhD, Han Jin Kwon PhD, Beom Joon Kim MD
- Efficacy and safety of PDLLA microsperes as subdermal fillers in animals. Chuan-Yuan Lin, Jui-Yu Lin, Dae-Yeol Yang, Seong-Ho Lee, Jeoung-Yong Kim, Miyeon Kang
- PDLLA membranes for bone regeneration. Marco Annunziata, DDS, PhD; Livia Nastri, DDS, PhD; Andrea Borgonovo, MD, DMD; Marco Benigni, DDS and Pier Paolo Poli DDS.
- Development and characterization of polymeric microparticle of PDLLA loaded with holmium acetylacetonate. Mariangela de Burgos M. de Azevedo, Vitor H. S. de Melo, Carlos Roberto J. Soares, Douglas M. Miyamoto, Ricardo A. Katayama, Peterson L. Squair, Caio H.N. Barros &Ljubica Tasic
- Assessment of the safety and efficacy of poly-L-lactic acid for treatment of HIV-associated facial lipoatrophy. Cheryl M. Burges, MD; and Rafaela M. Quiroga, MD
- Injectable poly-L-lactic acid for cosmetic enhancement: Learning from the European experience. Kimberly Butterwick, MD and Nicholas J. Lowe, MD FRCP
- Reconstruction of injectable PDLLA, Efficacy of different diluents and a new accelerating method. Se-Yi Chen, MD; Szu-Ting Chen, PhD; Jui-Yu Lin, MD; Chuan-Yuan Lin, MD
- Antibacterial poly (D,L-lactic acid) coating of medical implants using a biodegradable drug delivery technology. Hans Gollwitzer, Karim Ibrahim, Henriette Meyer, Wolfram Mittelmeier, Raymonde Busch and Axel Steberger
- Działanie kwasu polimlekowego w tkankach w chirurgii estetycznej. Dorota Małgorzata Wydro
- Biodegradable poly(DL-lactide-coglycolide) microspheres. J.H. Eldridge, J.K. Staas, T.R. Tice and R.M. Gilley
- Poly(D,L-lactic acid) nanoparticle size reduction increases its immunotoxicity. Jessica Da Silva, Sandra Jesus, Natalia Bernardi, Mariana Colaco and Olga Borges
- RGD-modified poly(D,L-lactic acid) nanoparticles enhance tumor targeting of oridonin. Jie Xu, Ji-Hui Zhao, Ying Liu, Nian-ping Feng, Yong-Tai Zhang
- The use of polylactic acid to obtain biodegradable medical devices. R.Yu. Galimzyanova, MD Mevliyanova, D.R. Hisamieva N.V. Pesternnikova, I.N. Musin and M.S. Lisanevich
- Injectable fillers for volume replacement in the aging face. Timothy M. Greco, M.D., F.A.C.S.; Marcelo B. Antunes, M.D.; Seth A. Yellin, M.D.
- Soft Tissue augmentation using sculptra. Gail Humble, M.D. and Douglas Mest, M.D.
- Efficacy and safety of injection with poly-L-lactic acid compared with hyaluronic acid for correction of nasolabial fold: a randomized, evaluator-blinded, comperative study. M.Y. hyun, Y. Lee, Y.A. No, K.H. Yoo, M.N. Kim, C.K. Hong, S.E. Chang, C.H. Won and B.J. Kim
- Preparation and characterization of microporous poly(D,L-lactic acid) film for tissue engineering scaffold. Shuai Shi, Xiu Hong Wang, Gang Guo, Min Fan, Mei Juan Huang, Zhi Yong Qian,
- Contolled cisplatin delivery system using poly(D,L-lactic acid). O. Ike, Y. Shimizu, R. Wada, S.-H Hyon and Y. Ikada
- Sculptra: A stymulatory filler. Victor Lacombe, M.D.
- Injectable PLLA (Sculptra) technical considerations in soft-tissue contouring. Samuel M. Lam, M.D., Babak Azizzadeh, M.D., Miles Graivier, M.D.
- Degradation of poly(D,L-lactic acid) nanoparticles coated with albumin in model digestive fluids (USP XXII). F.B. Landry, D.V. Bazile, G. Spenlehauer, M. Veillard and J. Kreuter
- Internalization of poly(D,L-lactic acid) nanoparticles by isolated human leukocytes and analysis of plasma proteins adsorber onto the particles. Jean_Christophe Leroux, Patricia Gravel, Lub Balant, Bernard Volet, Beatrice M. Anner, Eric Allemann, Eric Doelker and Robert Gurny.
- Biocompatibility of Poly_DL lactic acid (PDLLA) for lung tissue engineering. Y.M. Lin, A.R. Boccaccini, J.M. polak and A.E. Bishop
- Orofacial granulomas after injection of cosmetic fillers.Histopathologic and clinical study of 11 cases. T. Lombardii, J. Samson, F. Plantiere, C. Husson, R. Kuffer
- Long term (24-month) safety evaluation of PDLLA filler injection for the nasolabial fold. A multicenter, open, randomized, evaluator-blind, active-controlled design
- Optimizing poly-l-lactic acid use. Nick J. Lowe.
- The use of PDLLA devices for bone augmentation techniques: a systematic review. Marco Annunziata, Livia Nastri, Gennaro Cecoro and Luigi Guida
- Synthesis and characterization of low molecular weight polylactic acid. C.S. Proikakis, P.A. Tarantili and A.G. Andreopoulos
- Axonal regenration across an artificial scaffold combined with cel transplantation applied to the transected spinal cord. Mitsuhiro Enomoto, Madoka Ukegawa, Kazuyuki Fukushima, Kush Bhatt, Yoshiaki Wakabayashi, Atsushi Okawa
- Design of bioinspired polymeric materials based on poly (D,L-lactic acid) modifications toward improving its cytocompatibility. Xufeng Niu, Yanfeng Luo, Yonggang Li, Chunhua Fu, Jia Chen, Yuanliang Wang
- Biocompatibility and safety of PLA and its copolymers. Yuval Ramot, Moran Haim-Zada, Abraham J. Domb, Abraham Nyska
- Tamoxifen citrate-loaded poly(D,L) lactic acid nanoparticles: evaluation for their anticancer activity in vitro and in vivo. NR Ravikumara, Mausumi Bharadwaj and Basavaraj Madhusudhan.
- Poly-L-lactic acid: a new dimension in soft tissue augmentation. Adam M. Rotunda, Rhoda S. Narins
- A new option for volumetric restoration: poly-l-lactic acid. D Thioly-Bensoussan
- Drug-eluting biodegradable poly-D/L-lactic acid vascular stents: an experimental pilot study. Ilka Uurto, MD’ Joonas Mikkonen, MSc; Jyrki Parkkinen, MD; Leo Keski-Nisula, MD; Timo Nevalainen, DVM, Minna Kellomaki, MSc; Pertti Tormala, MSc; and Juha-Pekka Salenius, MD
- Facial Volumetric Correction with injectable poly-L-lactic acid. Danny Vleggaar, MD
- The use of poly-L-lactic acid in the management of soft-tissue augmentation: a five-year experience. Didier Vochelle, MD
- Molecular biocompability evaluation of poly(D,L-lactic acid)-modified biomaterials based on long serial analysis of gene expression. Yan Xiang, Yuanliang Wang, Yanfeng Luo, Bingbing Zhang, Juan Xin, Danfang Zheng
- The structure and properties of biodegradable PLLA/PDLA for melt-blown nonwovens. Bin yu, Yongmin Cao, Hui Sun, Jian Han
- Compositions of injectable poly D,L-lactic acid and injectable poly-L-lactic acid. S.Y. Chen, J.Y. Lin, C.Y. Lin in C”linical and Experimental Dermatology”.
- Foreign body reaction to poly-D-L-lactic acid resobable plates used in craniofacial surgery. Nicholas Cen, BS; Matthew J. Davis, BS; Amjed Abu-Ghname, BS; Lesley W. Davies, PA-C, Kalyani R. Patel, MD and Edward P. Buchanan, MD in „The Journal of Craniofacial Surgery”
- Comparison of antiaging effects on rat skin of COG thread and poly-L-lactic acid thread. Yelda Kapicioglu MD, Mehmet Gul PhD, Gulbahar Sarac MD, Birgul Yigitcan PhD and Harika Gozukara PhD
- Adverse reaction to polylactic acid injections in the periorbital area. M Apikian, FRACGP, S Roberts, FRACGP & G J Goodman FACD
- Dermal fillers for the traetment of tear trough deformity: a review of anatomy, traetment techniques, and their outcomes. Jaishree Sharad
- Foreign body granulomas after all injectable dermal fillers: part 1 . possible causes. Article in „Plastic and Reconstructive Surgery” – July 2009
- Preparation of poly (D,L) lactide microspheres by emulsion-solvent evaporation, and their clinical applications as a convenient embolic material. C. Grandfils, P. Flandroy, N. Nihant, S. Barbette, R. Jerome, Ph Teyssie and A. Thibaut
- A use of poly-L-lactide, D-lactide sheet on posteriori orbital floor fracture. Kun Hwang MD, PhD; Dong Hyun Kim, MD, MS and In Sun Park PhD
- Hanging by a thread: choosing the right thread for the right patient. Vincent Wong, Rafiq N. Kaylan R, Hsenriksen A, Funner R
- An approach to sstructural facial rejuvenation with fillers in women. R. Fitzgerald, MD, J. Carueville, MD, P.T. Yang, MD FRCSC
- A meta-analysis and systematic review of the incidences of complicattions following facial thread-lifting. Zehao Niu, Kexue Zhang, Wende Yao, Yan Li, Weiqian Jiang, Qixu Zhang, Maria J. Troulis, Meredith August, Youbai Chen, Yan Han.
- Our technique of thread lifting for facial rejuvenation. Irina Khrustaleva, MD, Galina Khrustaleva, MD, Anna Borovikova, MD, Alexey Tamarov, MD, Alexei Borovikov, MD
- Adverse reactions to injectable aesthetic micrimplants. Celia Requena, MD, Maria Jose Izquiderdo, MD, Miguel Navarro, MD, Antonio Martinez MD PhD, Juan Jose Vilata MD, PhD, Rafael Botella MD, PhD, Jorge Amorrortu, MD, Vicente Sabater MD, PhD, Adolfo Aliaga MD, PhD and Luis Requena MD, PhD
- Safety and complications of absorbable threads made of poly-L-lactic acid and poly lactide/glycolide: experience with 148 consecutive patients. Sukran Sarigul Guduk MD, Nezih Karaca MD
- Comperative effects of varius absorbable threads in a rat model. Jung Jin Shin, Tae Jun Park, Bo Young Kim, Chang Min Kim, Dong Hye Suh, Sang Jun Lee, Hye-Rim Moon & Hwa Jung Ryu
- Treatment of complications following facial thread-lifting. Youbai Chen, MD, PhD, MSc; Zehao Niu MD; Rui Jin MD; Yonghong Lei MD, PhD, Yan Han MD, PhD.
- Treatment of postblepharoplasty lower eyelid malposition by Aptos thread. Zuo Jun Zhao, MD; You Lu, BS; Wei Zhong Liang MD and Jun Ling Wu, BS
Publikacje dla zainteresowanych wysyłamy mailem, po przysłaniu tytułu wybranej publikacji.
